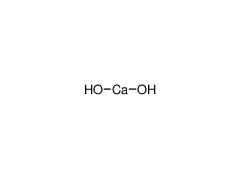
别名:熟石灰、消石灰
EINECS登录号215-137-3
熔点580 ℃(失水,分解)
沸点2850 ℃
水溶性微溶 (20℃时溶解度为1.65 g/L)
密度2.24 g/mL(25 ℃)
外观白色粉末状固体
应用水溶液可验证二氧化碳,建材
安全性描述S26;S39
危险性符号R41
危险性描述腐蚀性物品;刺激性物品
UN危险货物编号3262
酸碱性碱性
计算化学数据
1、疏水参数计算参考值(XlogP):无
2、氢键供体数量:2
3、氢键受体数量:2
4、可旋转化学键数量:0
5、互变异构体数量:无
6、拓扑分子极性表面积:2
7、重原子数量:3
8、表面电荷:0
9、复杂度:0
10、共价键单元数量:3
物理性质
密度(g/mL,25/4℃):2.24
氢氧化钙在常温下是细腻的白色粉末,微溶于水,其澄清的水溶液俗称澄清石灰水,与水组成的乳状悬浮液称石灰乳。且溶解度随温度的升高而下降。不溶于醇,能溶于铵盐、甘油,能与酸反应,生成对应的钙盐。580℃时,分解为氧化钙和水。
对于氢氧化钙的溶解度随着温度升高而降低的问题,主流的解释是,因为氢氧化钙有两种水合物〔Ca(OH)2·2H2O和Ca(OH)2·12H2O〕。这两种水合物的溶解度较大,无水氢氧化钙的溶解度很小。随着温度的升高,这些结晶水合物逐渐变为无水氢氧化钙,所以,氢氧化钙的溶解度就随着温度的升高而减小。
化学性质
碱性
氢氧化钙是强碱,对皮肤、织物有腐蚀作用。但因其溶解度不大,所以危害程度不如氢氧化钠等强碱大。氢氧化钙能跟酸碱指示剂作用:
紫色石蕊试液遇氢氧化钙显蓝色,无色酚酞试液遇氢氧化钙显红色。
化学方程式
1、氢氧化钙与二氧化碳反应:
CO2+Ca(OH)2=CaCO3↓+H2O
2、氢氧化钙与酸反应,生成盐和水。
稀盐酸与氢氧化钙反应:
2HCl+Ca(OH)2=CaCl2+2H2O
3、氢氧化钙与某些盐反应,生成另一种碱和另一种盐。
碳酸钠溶液与氢氧化钙反应:
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
硝酸铵与氢氧化钙反应:
2NH4NO3+Ca(OH)2=2NH3↑+2H2O+Ca(NO3)2
氯化镁与氢氧化钙反应:
MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓
毒理学数据
急性毒性:大鼠口经LD50:7340mg/kg;小鼠口经LD50:7300mg/kg。
属强碱性物质,有刺激和腐蚀作用。吸入粉尘,对呼吸道有强烈刺激性,还有可能引起肺炎。眼接触亦有强烈刺激性,可致灼伤。
安全信息
安全措施
健康危害
氢氧化钙粉尘或悬浮液滴对黏膜有刺激作用,能引起喷嚏和咳嗽,和碱一样能使脂肪皂化,从皮肤吸收水分、溶解蛋白质、刺激及腐蚀组织。吸入石灰粉尘可能引起肺炎。
人体过量服食和吸收氢氧化钙会导致有危险的症状,例如呼吸困难、内出血、肌肉瘫痪、低血压、阻碍肌球蛋白和肌动蛋白系统,增加血液的pH值,导致内脏受损等。
急救措施
皮肤接触:应立即用大量水冲洗,再涂上3%-5%的硼酸溶液。
眼睛接触:立即提起眼睑,用流动清水或生理盐水冲洗至少15分钟。或用3%硼酸溶液冲洗。就医。
吸入:迅速脱离现场至空气新鲜处。必要时进行人工呼吸,就医。
食入:应尽快用蛋白质之类的东西清洗干净口中毒物,如牛奶、酸奶等奶质物品。患者清醒时立即漱口,口服稀释的醋或柠檬汁,就医。
危害防治
呼吸系统防护:必要时佩带防毒口罩。
眼睛防护:戴化学安全防护眼镜。
防护服:穿工作服(防腐材料制作)。
手防护:戴橡皮手套。
其它:工作后,淋浴更衣。注意个人清洁卫生。
安全术语
S26:不慎与眼睛接触后,请立即用大量清水冲洗并征求医生意见。
S37:戴适当手套。
S39:戴护目镜或面具。
风险术语
R41:对眼睛有严重伤害。
储存运输
运输方法
起运时候包装要完好,装载应稳妥。运送过程之中要保证容器不走漏、不坍毁、不掉落、不损坏。严禁和易燃物或可燃物、酸类、食用化学品等混装混运。雨天不宜运送。
储存方法
贮存于阴凉、通风的仓库。库内湿度最佳不大于85%。包装有必要完好密封,避免吸潮。应与易(可)燃物、酸类等分隔寄存,切忌混储。储区应该备有适宜的资料收留泄漏物。
合成方法
工业制备
1、石灰消化法
将石灰石在煅烧成氧化钙后,经精选与水按1:(3~3.5)的比例消化,生成氢氧化钙料液经净化分离除渣,再经离心脱水,于150~300℃下干燥,再筛选(120目以上)即为氢氧化钙成品。
CaCO3→CaO+CO2↑
CaO+H2O→Ca(OH)2。
2、将试剂氯化钙溶于水中,制得25%的水溶液,加热至80℃,然后分次加入滤过的30%的氢氧化钠溶液 ( 可超过理论量30%) ,反应得到氢氧化钙,所得浆状混合物经抽滤后洗涤,先用0.1%的氢氧化钠水溶液洗去大量氯离子,然后用蒸馏水洗至氯离子合格。
3、扩散法
首先配制两种溶液:一为30g重结晶的CaCl2·6H2O溶于50mL水中;一为12gNaOH溶于50mL水并滴加少量Ba(OH)2的沉淀碳酸盐。将两种溶液分别装满两个50mL的烧杯中。将两个烧杯小心地放在同一个容器中,烧杯距离容器的上缘2cm,盖好容器盖,静置4周后有1cm左右的针状结晶生长出来,收集过滤,快速水洗,再依次用稀盐酸、水、乙醇、乙醚洗涤,最后在短时间内于110℃进行干燥。
4、将碱金属的氢氧化物溶液与钙盐的水溶液作用可得氢氧化钙。将46g四水硝酸钙溶于经过煮沸排除气体的500mL的蒸馏水中,冷却至0℃,边振荡边分多次加入1mol/L的氢氧化钾溶液(不含CO2),滴加过程中保持溶液为0℃,过滤分离析出的Ca(OH)2沉淀,用12L水分若干次倾析洗涤,吸滤沉淀在硫酸(相对密度1.355)干燥器中真空干燥20h可得Ca(OH)2。
实验室制备
将生石灰(CaO)放入烧杯加入水。氧化钙和水反应,放出热量,生成物是氢氧化钙。反应式:CaO+H2O→Ca(OH)2。
用途
1、可作生产碳酸钙的原料。
2、氢氧化钙属碱性,因而可以用于降低土壤的酸性,从而起到改良土壤结构的作用。农药中的波尔多液正是利用石灰乳(溶于水的氢氧化钙)和硫酸铜水溶液按照一定的比例配制而出的。冬天,树木过冬防虫,树木根部以上涂80公分的石灰浆。
3、优质品主要用于生产环氧氯丙烷、环氧丙烷。
4、可用在橡胶、石油化工添加剂中,如石油工业加在润滑油中,可防止结焦、油泥沉积、中和防腐。
5、用于制取漂白粉、漂粉精、消毒剂、制酸剂、收敛剂、硬水软化剂、土壤酸性防止剂、脱毛剂、缓冲剂、中和剂、固化剂等。
6、氢氧化钙和空气中二氧化碳还会发生反应从而形成难溶于水的碳酸钙。制糖工业生产中,先利用氢氧化钙中和糖浆中的酸,然后通入二氧化碳和剩余氢氧化钙反应生成沉淀物被过滤出去,以此减少糖的酸味。